Страница 1 из 5
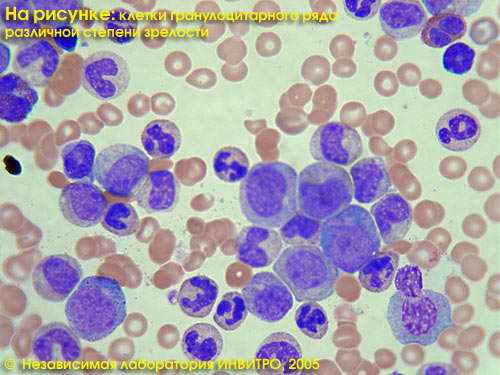
Острые лейкозы — это самые опасные и стремительные болезни крови. При острых лейкозах происходит поломка на уровне самых молодых клеток крови, клеток-предшественников, клеток-бластов, которые являются одним из подвидов белых кровных телец, лейкоцитов. Слово бласт происходит от слова blastos, что по-гречески означает «росток, зародыш, побег». Бласты — это быстро растущие клетки. Здоровая бластная клетка со временем развивается в какую-либо полезную клетку крови. В норме число бластов не превышает 1% от всех клеток костного мозга. В кровь они почти никогда не выходят. Если человеку срочно понадобилось большое число каких-нибудь клеток крови (например, лейкоцитов при тяжелой инфекции), то бластов организм может вырабатывать и больше, но все же их относительное число редко превышает 10%.
Бласты, которые размножаются при остром лейкозе, другие. Их можно сравнить с хулиганами-тунеядцами в человеческом обществе, потому что они не работают, питаются запасами организма и вместо собственного развития в полезные клетки быстро плодят себе подобных. Лейкозные бласты вытесняют здоровые клетки крови из их дома внутри костей и поселяются там сами. Из-за этого нарушается процесс обновления нормальной крови, начинается ее дефицит: быстро снижается гемоглобин, тромбоциты, здоровые лейкоциты. Пациент начинает слабеть, могут появиться самопроизвольные кровотечения и высокая температура. В анализе крови врач видит снижение гемоглобина и тромбоцитов и резкое повышение лейкоцитов за счет опухолевых клеток-бластов. Больше всего опухолевых клеток в костном мозге.
Принципиально врачи выделяют два типа бластов: лимфобласты и миелобласты. В зависимости от типа бластов и лейкозы бывают лимфобластные и миелобластные (нелимфобластные). Это зависит от того, в начале какого из двух путей развития клетки крови произошла авария.
В норме из здоровых лимфобластов (клеток-предщественников) образуются высокоспециализированные клетки иммунной системы В- и Т- лимфоциты. Задачи В- и Т-клеток можно сравнить с задачами войск специального назначения, которые действуют точно и эффективно. Из миелобластов в дальнейшем получаются остальные виды клеток: красные кровяные тельца, тромбоциты, гранулоциты. Красные кровяные тельца (эритроциты) — переносят кислород, тромбоциты отвечают за свертывание крови, если мы, например, поранились. Гранулоциты — «общевойсковая» часть иммунной системы, они действуют более массированными ударами.
Если произошла поломка, то нормальные клетки не созревают, а бласты остаются недоразвитыми. По внешнему виду бласта, а также с помощью проточной цитометрии можно определить, какая клетка могла бы из него получиться. Это важно для выбора лечения и понимания, насколько успешным будет лечение. Вид клеток-предшественников врачи обозначают в диагнозе, например: острый В-лимфобластный лейкоз (лейкоз из клеток-предшественников В-лимфоцитов), острый монобластный лейкоз (лейкоз из клеток-предшественников моноцитов) и т.д.
Диагноз «острый лейкоз» ставят, если выясняют, что бластов в костном мозге пациента более 20%. Чтобы понять, какой именно лейкоз у больного, делают проточную цитометрию бластов.
Острые лейкозы бывают очень разные. Лейкоз, например, может появиться «на ровном месте», то есть у человека, у которого никогда не было никаких болезней страшнее насморка. Такими лейкозами обычно болеют дети и молодые люди. У людей старшего возраста острые лейкозы, как правило, вторичны. Это значит, что в результате каких-то причин (химиотерапия по поводу других болезней, облучение или отравление некоторыми химическими веществами) может нарушиться кроветворение, то есть появляется так называемый миелодиспластический синдром (мы уже описывали его в других разделах нашего сайта). Последней ступенью миелодиспластического синдрома является вторичный острый лейкоз. Первичные лейкозы более агрессивны, чем вторичные, но все лейкозы лечат по единым принципам. Чтобы полностью вылечить пациента, часто необходимо сделать пересадку донорских стволовых клеток крови.
О некоторых типах острых лейкозов мы расскажем в этой главе:
- острый миелобластный лейкоз;
- острый лимфобластный лейкоз;
- миелоидная саркома;
острые лейкозы смешанного фенотипа.
Как распознать лейкоз по анализу крови?
Врач-гематолог, доктор медицинских наук Сергей Семочкин про острый лимфобластный лейкоз

Врач-гематолог, профессор кафедры онкологии, гематологии и лучевой терапии РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук Сергей Семочкин рассказал: можно ли распознать острый лимфобластный лейкоз (ОЛЛ) на ранней стадии и поставить диагноз по анализу крови; объяснил, как лечат ОЛЛ и кому показана трансплантация костного мозга (ТКМ).
Каковы ранние симптомы острого лимфобластного лейкоза? Можно ли их увидеть и распознать ОЛЛ?
В данном случае все достаточно просто, потому что слово «острый» означает, что заболевание внезапное и зачастую симптомы очень выразительные. Самый частый симптом — это лихорадка, т.е. повышение температуры тела. Лихорадка может быть как субфебрильной, так и ярко выраженной, до 39 градусов. Появятся изменения, связанные с поражением костного мозга. Снижение гемоглобина приведет к слабости и быстрой утомляемости. Могут увеличиться лимфатические узлы, появиться дискомфорт в брюшной полости за счет того, что увеличиваются размеры печени и селезенки. Могут быть проявления кровоточивости — даже во время чистки зубов. У некоторых пациентов ОЛЛ может начаться с неврологических проявлений — головных болей, головокружения и прочих проблем. Симптоматика обширная, но в данном случае она является достаточно острой, внезапно возникшей.
Смотрите видео на нашем сайте.
Можно ли поставить диагноз по анализу крови? Что он покажет?
Как правило, в анализе крови есть ярко выраженные показатели: изменены ростки кроветворения, количество лейкоцитов выходит за пределы нормы — может упасть ниже нормальных значений, а может стать запредельно огромным. Мне встречались пациенты, у которых количество лейкоцитов при норме от 4 до 9 тысяч повышалось до 200 тысяч на мкл. Тромбоциты тоже в ряде случаев очень сильно снижены, но главное — изменение количества лейкоцитов. Очень важным маркером является выход опухолевых клеток в кровь, когда в крови появляются незрелые ранние клетки, которые называют бластными. Если в анализе крови выявили бластные клетки, то это, скорее всего, либо острый лейкоз, либо миелодиспластический синдром.
Как пациент попадает к гематологу?
Анализ крови с характерными изменениями — повод для немедленного вызова скорой помощи и госпитализации пациента в профильный стационар. При лечении детей и подростков у онкогематолога, как правило, есть один-два дня ни диагностику, лечение необходимо начинать, как можно раньше. В диагностику входит повторный анализ крови, затем — верификация диагноза, для которой проводят биопсию костного мозга. У маленьких детей ее проводят под общей анестезией, у взрослых — под местной. С помощь небольшой иглы делаю прокол грудины или подвздошной кости. У детей пункцию грудины не делают. Полученный образец костного мозга, который выглядит как обычная пробирка с кровью, отправят в лабораторию, где для подтверждения диагноза проведут целый спектр исследований. Главный критерий — увеличение количества бластных клеток. Только по внешнему виду и по количеству бластных клеток определить вариант лейкоза — невозможно. Еще в 1913 году установили, что есть лимфоидный, а есть миелоидный вариант лейкоза. Для верификации применяются специальные лабораторные методы: иммунологические и химические. Существует специальный прибор — проточный цитометр, с помощью которого определяют маркеры, характеризующие данный тип клеток. Для определения подвида острого лейкоза, применяют целый спектр генетических исследований, чтобы выйти на более целевую терапию у этих пациентов.
Каковы причины возникновения ОЛЛ? Существует мнение, что этот вид лейкоза очень сильно взаимосвязан с экологическими проблемами, передается по наследству и часто возникает у тех, кто уже переболел каким-то онкологическим заболеванием. Правда это или нет?
Истинную причину возникновения лейкоза у взрослых можно выявить только в 5% случаев, в 95% совершенно непонятно, что там к чему привело. У детей все несколько интересней.
Как возникает лейкоз? В генетическом материале клетки возникает некая первичная мутация, которая сама по себе далеко не всегда приводит к лейкозу. В дальнейшем к этой мутации присоединяются другие, и когда болезнь все же возникает, в клетке накоплено уже много молекулярных событий, сочетание которых привело возникновению заболевания. Пик острого лимфобластного лейкоза приходится на детей от двух до четырех лет, потом заболеваемость падает. Следующий пик приходится на 18-29 лет, потом снова спад. После 60 лет — опять небольшой рост.
У части детей раннего возраста прослеживается некая врожденная составляющая этой проблемы. Встречаются случаи ОЛЛ у плода или новорожденного, когда ребенок рождается уже с заболеванием, либо заболевает в течение первого года жизни. Исследования пуповинной крови показали, что у новорожденных встречаются лейкемические поломки, врожденные мутации, которые могут привести к возникновению лейкоза. И мутацию эту вызывает наследственный фактор, сработавший во время внутриутробного развития. По разным данным, общее количество таких младенцев составляет от 1 до 5%. Дальше многое зависит от инфекционной обстановки, сложившейся вокруг ребенка. Многочисленные инфекции, перенесенные в детстве, способствуют формированию нормальной иммунной системы, которая нейтрализует наследственный фактор.
Если говорить про экологические проблемы, то с ними четкой связи не выявлено.
Влияет ли УФ-излучение, СВЧ, солнечные лучи, радиация?
В Хиросиме и Нагасаки повышенная заболеваемость держалась около 12 лет. После Чернобыля у многих пострадала щитовидная железа, но заболеваемость лейкозами не выросла. Все зависит от типа изотопов попавших в окружающую среду. В Фукусиме тоже этого не случилось, потому что концентрация радиоактивных веществ сильно разбавилась морской водой.
Вред ультрафиолета научно доказан только в отношении меланомы. Четкой связи с ОЛЛ нет. Своим бывшим пациентам мы не разрешаем посещать солярий и не рекомендуем загорать, потому что хотя связь и не доказана, совсем исключать этот фактор тоже нельзя.
Если говорить об СВЧ-излучении, домашние микроволновые печи абсолютно безопасны.
Как лечат ОЛЛ? Что ждет пациента?
Концепция лечения ОЛЛ, которая до сих поре лежит в основе протоколов лечения ОЛЛ, была разработана американским педиатром Дональдом Пинкелем еще в 1962 году. Она включает в себя четыре этапа: индукция ремиссии, консолидация, воздействие на центральную нервную систему и длительный этап поддерживающей терапии на протяжении двух-трех лет. Во всем мире проводится лечение по клиническим протоколам, разработанным в результате кооперированных исследований. Согласно некоторым работам, строгое следование протоколам повышает выживаемость пациентов на 15-20% по сравнению с индивидуализированным лечением. В протоколе прописаны все действия: от первого дня до последнего. В нем есть указания, как и в какой момент оценивать возникающие осложнение и что с ними делать. В России два центра, активно ведущих такие протоколы. Центр им. Дмитрия Рогачева, где Александр Исаакович Карачунский в течение многих лет, с начала 1990-х, ведет серию протоколов «Москва — Берлин». Каждые пять лет дизайн протоколов пересматривают, чтобы улучшить лечение отдельных категорий пациентов. уже в течение многих лет с начала 90-х годов серию протоколов Москва-Берлин. Каждые пять лет меняется дизайн протоколов, направленных на улучшение лечения отдельных категорий пациентов. Во взрослой практике — это НМИЦ гематологии, где ведут кооперированные исследования по острому лимфобластному лейкозу у взрослых.
В каких случаях показана трансплантация костного мозга (ТКМ)?
В отличие от острого миелоидного лейкоза, показаний к аллогенной (от донора) ТКМ меньше. Ее назначают пациентам, которые не достигли ремиссии в указанные протоколом сроки или имеют неблагоприятный цитогенетический вариант заболевания. В детской практике выздоравливают более 90% детей, и примерно 15-20% являются кандидатами для аллогенной ТКМ. У взрослых процент пациентов нуждающихся в трансплантации несколько выше, за счет того, что генетических операций высокого риска становится намного больше и ответ на стандартное лечение хуже. Когда мы обсуждали хронический миелолейкоз, там фигурировала филадельфийская хромосома — транслокация (9;22). При ОЛЛ это абсолютно негативный фактор прогноза. У детей такая мутация встречается меньше чем в 5% случаев, у людей старше 50-60 лет примерно половина В-линейных ОЛЛ будет с филадельфийской хромосомой. В отличие от хронического миелолейкоза, применение ингибиторов тирозинкиназы при остром лимфобластном лейкозе не столь успешно. Вот поэтому во взрослой практике ТКМ необходимо проводить примерно 30% пациентов. Возрастной порог для аллогенной ТКМ — в районе 55 лет, это разумно.
Как часто случаются рецидивы с ОЛЛ?
Если мы говорим про взрослых людей, то рецидивы случаются почти в 40% случаев. Бывают ранние рецидивы, которые случаются прямо на терапии. В таком случае необходимо менять лечение, делать его более интенсивным и тяжелым. В таких случаях, как правило, показана ТКМ. Поздний рецидив может случиться и через 20 лет. К сожалению мы не можем убрать причину, которая вызывает это заболевание — оно может вернуться.
Можно ли планировать беременность после ОЛЛ?
Длительная химиотерапия нарушает фертильность, поэтому лучше провести криоконсервацию спермы/яйцеклетки, а еще лучше эмбриона — это более надежный способ. У мужчин, как правило, серьезно нарушается сперматогенез, но у женщин дело обстоит несколько лучше. Вероятность забеременеть и выносить здорового ребенка высока. Если прошло не менее пяти лет в ремиссии, никаких ограничений нет.
Может ли беременность быть провоцирующим фактором для рецидива?
Скорее, нет. Это не такое частое явление, как при некоторых других заболеваниях, где беременность действительно может стать провоцирующим фактором.
Передается ли ОЛЛ по наследству?
Лимфобластный лейкоз — редкое заболевание, поэтому вероятность того, что он случится у ребенка, рожденного от родителей после ОЛЛ, крайне мала.
Как будут лечить ОЛЛ в будущем?
Представляется, что в основе лечения онкологических заболеваний в будущем станет активация собственного иммунитета. Нам необходимо настроить иммунную систему таким образом, чтобы она распознавала и убирала раковые клетки. Сейчас мы находимся на раннем этапе развития CAR-T-терапии, но через какое-то время технологии настолько усовершенствуются, что, скорее всего, она станет одним из основных методов терапии при целом ряде онкогематологических заболеваний. Суть метода заключается в том, что у пациента собирают его собственные Т-лимфоциты и отправляют в специальную лабораторию. Эта лаборатория может быть в другом городе, стране — не важно. В лаборатории эти Т-лимфоциты перепрограммируются: в них появляется информация об опухолевых клетках, присутствующих в организме пациента. После перепрограммирования Т-лимфоциты вводят обратно пациенту, она находят раковые клетки и возникает ремиссия. Основные проблемы — создать качественный процесс распознавания и разработать стандартные протоколы лечения.
Много вопросов возникает в понимания биологии заболевания, потому как каждый конкретный случай весьма индивидуален. Мы знакомы только с грубыми поломками, но каждая отдельная поломка провоцирует различное течение болезни. Мы уже сейчас можем полностью секвенировать геном опухолевой клетки и главное научиться понимать, что в патогенезе является ключевым и как на это можно воздействовать, тогда мы ближе подойдем к полному излечению болезни. За этим будущее.
Болезни крови: диагностика и лечение
Как утверждает энциклопедия, кровь — это жидкая подвижная соединительная ткань, которая состоит из плазмы и взвешенных в ней гемопоэтических клеток.
С древнейших времен она вызывала большой интерес у ученых мужей, ей предписывались колдовские свойства, а над разгадками ее тайн бились лучшие умы человечества. И сегодня медицина уделяет крови и системе кроветворения огромное внимание, им посвящен отдельный раздел медицинской науки — гематология, о которой расскажет врач-гематолог высшей категории, доктор медицинских наук, главный специалист Министерства здравоохранения, труда и социальной защиты Молдовы в области злокачественных заболеваний системы крови Василий Мустяцэ.
 Василий Мустяцэ,
Василий Мустяцэ,
врач-гематолог высшей категории,
доктор медицинских наук,
главный специалист
Министерства здравоохранения, труда
и социальной защиты РМ в области
злокачественных заболеваний системы крови
Расскажите, пожалуйста, что такое гематология?
Гематология — это раздел медицины, изучающий заболевания системы кроветворения (гематопоэза) и занимающийся их диагностикой и лечением.
Что представляет собой кроветворная система?
Ее составляющими является костный мозг, лимфатические узлы, селезенка, а также некоторые другие органы и ткани. В костном мозге происходят образование и созревание клеток крови. Здесь клетки-предшественники переходят в более зрелые формы, образуя два различных ростка кроветворения — лимфоидный (лимфоциты) и миелоидный (гранулоциты, эритроциты, тромбоциты).
Лимфоузлы производят лимфоциты и плазматические клетки — агенты иммунной системы. Селезенка — самое большое хранилище эритроцитов в организме, кроме того она продуцирует лимфоциты и активно участвует в работе иммунной системы.
Какие существуют болезни крови?
Все заболевания системы кроветворения делятся на доброкачественные и злокачественные. К доброкачественным, главным образом, относятся различные формы анемий и геморрагические диатезы, включающие в себя обширную группу наследственных или приобретенных заболеваний системы кроветворения, при которых наблюдается повышенная склонность к кровоточивости. Злокачественные болезни системы крови подразделяются на лейкозы и лимфомы.
В свою очередь лейкозы делятся на острые и хронические с учётом того, в каких родоначальных клетках произошла опухолевая мутация. Среди злокачественных лимфом выделяют лимфому Ходжкина и неходжкинские лимфомы. Важно отметить, что онкогематологические недуги характеризуются злокачественной трансформацией клеток кроветворной системы с последующим формированием опухолевого клона и дальнейшим его распространением гематогенным или лимфогенным путем (по крови или лимфе) в различные ткани и органы.
Давайте несколько подробнее остановимся на вышеназванных недугах. Что они представляют собой?
 Лейкозы — группа заболеваний, характеризующихся первичным поражением костного мозга. Как я уже сказал, они бывают острыми и хроническими. В зависимости от типа измененных клеток лейкозы подразделяются на лимфоидные и миелоидные.
Лейкозы — группа заболеваний, характеризующихся первичным поражением костного мозга. Как я уже сказал, они бывают острыми и хроническими. В зависимости от типа измененных клеток лейкозы подразделяются на лимфоидные и миелоидные.
В свою очередь они делятся на множество подвидов, отличающихся друг от друга своими морфологическими, иммунологическими и генетическими свойствами. При острых лейкозах молодые (бластные) клетки крови утрачивают способность дифференцироваться до зрелых форм и постепенно замещают собой здоровые клетки крови.
Поскольку бластные клетки постоянно образуются в костном мозге, то болезнь прогрессирует стремительно. Хронические формы лейкоза представлены преимущественно классом созревших клеточных структур, при этом опухолевые клетки по своему виду будут напоминать нормальные. Однако их жизненный цикл нарушается — становится излишне продолжительным, что мешает нормальной выработке здоровых клеток.
Острые лейкозы отличает агрессивный дебют с ярковыраженными признаками недуга. Хронические — постепенное начало. Какое-то время болезнь может себя практически не проявлять. Однако на определенном этапе заболевания в опухолевом клоне происходят новые мутации, с которыми иммунная система перестает справляться, и тогда клиническая картина разворачивается в полном объеме и больной испытывает весь спектр симптомов, характерных для лейкоза. Важно отметить, что острый лейкоз никогда не переходит в хроническую форму, а хронический не трансформируется в острый.
Профилактика
Каких-либо специфических мер нет. Здоровый образ жизни и регулярные профилактические обследования (при отсутствии жалоб общий анализ крови необходимо сдавать не реже одного раза в год) — вот, что можно посоветовать. Помните, что любое заболевание, выявленное на ранних этапах, поддается лечению гораздо лучше. Современная медицина достигла высоких результатов в терапии онкогематологических болезней, и с уверенностью могу сказать: злокачественные заболевания крови — это не приговор, а только диагноз!
Каким образом осуществляется диагностика?
В случаях с лейкозами — на основании анализов крови и костного мозга. При выявлении злокачественных лимфом пациентам проводится ряд исследований крови, а также выполняется биопсия поражённого лимфоузла (у больного удаляется поражённый лимфоузел для последующего морфологического исследования).
Как проводится лечение злокачественных болезней крови?
Лечение лейкозов и лимфом — сложный и длительный процесс, который может занять несколько лет. Для достижения оптимального результата очень важно строго следовать всем рекомендациям врача. Острые лейкозы лечатся химиотерапевтическими препаратами, хронические — химио- и иммунотерапией. При злокачественных лимфомах применяют химио-, радио- и иммунотерапию.
В случаях, когда болезнь отличает стойкое течение и она не отвечает на классические протоколы лечения, пациентам необходимо проводить пересадку гомопоэтических стволовых клеток (трансплантацию костного мозга). Эта сложная процедура, к сожалению, в нашей стране до сих пор не выполняется. Однако в настоящее время в Онкологическом институте разработан проект по созданию центра трансплантации костного мозга, есть обширные знания и накопленный опыт, которые мы готовы применять на практике.
А что касается злокачественных лимфом?
Сам термин «злокачественная лимфома» обозначает «злокачественное увеличение лимфатических узлов». Он включает в себя большую группу онкологических заболеваний лимфатической системы. Злокачественные лимфомы возникают из лимфоидных клеток, расположенных вне костного мозга.
В отличие от лейкозов, они характеризуются наличием первичного опухолевого очага (нередко пациент сам обнаруживает у себя «шишку», которая при проверке оказывается злокачественной лимфомой). Кроме того, данные новообразования способны как к метастазированию, так и к диссеминированию («рассеиванию» по всему организму).
Как уже было сказано, выделяют лимфому Ходжкина (лимфогранулематоз, болезнь Ходжкина) и большую группу неходжкинских лимфом. Почти 50% лимфом первично локализуются в лимфатических узлах, однако они могут поражать любые органы, где есть лимфатическая ткань. При поражении периферических лимфоузлов наиболее часто в процесс вовлекаются лимфатические узлы шеи и надключичной области.
Что говорит статистика, как обстоят дела с онкогематологическими заболеваниями в нашей стране?
В структуре заболеваемости среди онкологических болезней онкогематологические занимают пятое место. Из общего количества онкобольных на онкогематологических пациентов приходится около 6,6%. В 2018 году в республике Молдова (с учетом Приднестровского региона) было зарегистрировано 4113,5 случая, что касается правобережья -3547,5. Если говорить о маленьких пациентах, то в нашей стране на сегодняшний день насчитывается 260 детей, страдающих от злокачественных заболеваний крови. Ежегодно среди детского населения регистрируется 40-42 новых случаев.
В каком возрасте могут возникать злокачественные болезни системы крови?
В любом. Примечательно, что они более распространены среди представителей сильной половины человечества.
Когда необходимо обращаться к врачу-гематологу?
Далеко не каждый «плохой» анализ — это повод для серьезных опасений, ведь на соотношение клеток крови могут влиять многие инфекционные заболевания, лекарственные средства, аллергены, образ
питания и даже серьезное переутомление. Поэтому решение о необходимости консультации гематолога должен принимать семейный врач. Если пациент предъявляет характерные жалобы, а в общем анализе крови выявлены определенные нарушения, то тогда он получает направление на прием к специалисту в онкологическую поликлинику.
С какими симптомами сталкивается заболевший?
При лейкозах и лимфомах они различны. При лейкозах человек испытывает слабость, быструю утомляемость, у него без видимых причин повышается температура, возникают боли в костях, суставах и мышцах, на теле могут появляться синяки или мелкие кровоподтеки, кровоточат десны, нередко начинаются носовые кровотечения, увеличиваются лимфоузлы. Кроме того, больные становятся чрезмерно восприимчивыми к инфекционным заболеваниям, при этом их выздоровление серьезно затягивается.
Нередко острые лейкозы начинаются, как банальный грипп или ОРВИ. При лимфомах отмечается повышенная потливость (особенно в ночное время), резкое снижение массы тела, возможен кожный зуд, необъяснимые подъемы температуры тела выше 38°С. Обязательный и самый главный признак — последовательное увеличение лимфоузлов, при этом они плотные, безболезненные, не спаянные с окружающими тканями, часто сливаются в конгломераты. В ряде случаев появление одного или нескольких из указанных симптомов может опережать развитие самой опухоли.
Каковы причины возникновения онкогематологических заболеваний?
На этот вопрос с точностью ответить невозможно, однако к вероятным предпосылкам относят воздействие ионизирующего излучения, контакты с рядом химических веществ, стрессы, иммунодефицитные состояния, некоторые вирусные инфекции. Определенную роль играет наследственность и привычный образ жизни, бесконтрольное употребление лекарственных средств, плохая экологическая обстановка,
список можно продолжать долго. На самом деле достаточно редко удается обнаружить точную причину, которая стала механизмом, запустившим недуг.
Текст: Мария Брайлян
- Baas, «Geschichte d. Medicin».
- Puccinotti, «Storia della medicina» (Ливорно, 1954—1959).
- Baas, «Geschichte d. Medicin».
- https://www.spbsverdlovka.ru/patsientam/biblioteka-patsienta/patienth5.html.
- https://leikozu.net/faq-rak/kak-raspoznat-lejkoz-po-analizu-krovi/.
- https://sanatate.md/leikoz-limfoz-diagnostika-lecenie/.
- Moustafine R. I., Bukhovets A. V., Sitenkov A. Y., Kemenova V. A., Rombaut P., Van den Mooter G. Eudragit® E PO as a complementary material for designing oral drug delivery systems with controlled release properties: comparative evaluation of new interpolyelectrolyte complexes with countercharged Eudragit® L 100 copolymers. Molecular Pharmaceutics. 2013; 10(7): 2630–2641. DOI: 10.1021/mp4000635.
- Киржанова Е. А., Хуторянский В. В., Балабушевич Н. Г., Харенко А. В., Демина Н. Б. Методы анализа мукоадгезии: от фундаментальных исследований к практическому применению в разработке лекарственных форм. Разработка и регистрация лекарственных средств. 2014; 3(8): 66–80. DOI: 10.33380/2305-2066-2019-8-4-27-31.
- ОФС.1.2.1.1.0003.15 Спектрофотометрия в ультрафиолетовой и видимой областях // Государственная фармакопея, XIII изд.
- Pund A. U., Shandge R. S., Pote A. K. Current approaches on gastroretentive drug delivery systems. Journal of Drug Delivery and Therapeutics. 2020; 10(1): 139–146. DOI: 10.22270/jddt.v10i1.3803.